Modéliser le réel pour prendre en compte sa complexité
Parce que le corps humain est complexe et variable, il arrive que des patients répondent mal ou de façon non optimale à un protocole médical pourtant bien connu. L’idéal serait de pouvoir bénéficier d’une médecine réellement personnalisée, étudiant chaque patient de manière détaillée avant toute intervention ou prescription médicamenteuse. Si un tel degré d’analyse est encore utopique, la modélisation mathématique permet déjà de faire avancer la compréhension médicale en identifiant les mécanismes à l’œuvre dans les pathologies et en testant virtuellement des hypothèses et traitements.
Faire dialoguer les expertises pour relier les échelles micro et macro
C’est la mission que se sont fixée Dirk Drasdo et Irene Vignon-Clementel, tous deux directeurs de recherche au centre Inria de Saclay. Ensemble, ils coordonnent l'équipe SimbiotX (SImulations in Medicine, BIOtechnology and ToXicology of multicellular systems). Le premier apporte à l’équipe sa compétence en modélisation de tissus multicellulaires, établis à partir de données d’imagerie à l’échelle tissulaire. Quantitatifs et dynamiques, ses modèles permettent de suivre l’évolution spatiotemporelle de systèmes in vitro et in vivo, de la cellule individuelle au bloc de tissu. Ceux-ci se combinent avec les méthodes macroscopiques de simulation du flux sanguin in vivo, développées par sa collègue. Le résultat : des modèles hybrides qui font progresser la compréhension du lien entre ce qui se passe à l’échelle microscopique, cellulaire, et les conséquences macroscopiques, systémiques.
Les deux chercheurs ont ainsi réussi à montrer qu’on pouvait rapprocher des coupes de tissus tumoraux et des données obtenues par certaines méthodes d’imagerie. Grâce à la compréhension de cette relation, les modèles in silico seront paramétrés pour qu’ils reflètent l’architecture, la perfusion et la fonction des organes observés par imagerie. À terme, en combinaison avec l’analyse de différents biomarqueurs d’intérêt, cette avancée pourrait permettre le diagnostic tumoral en réduisant le recours à des modalités d’analyse invasives, telles que les biopsies. En améliorant la compréhension de la progression de la maladie, ces modèles aideront également à en planifier les traitements.
Jumeau numérique : vérifier in silico les hypothèses scientifiques
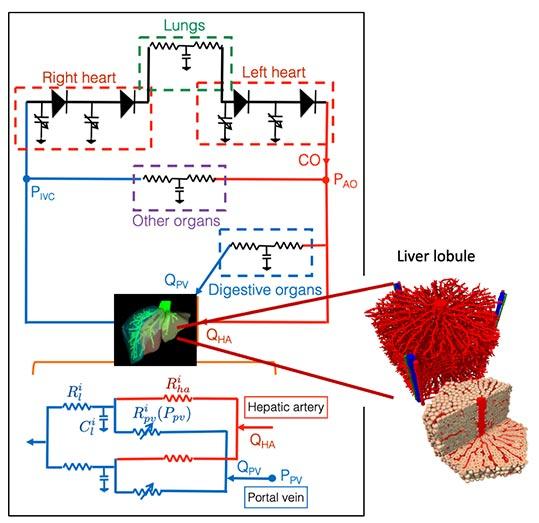
L’approche développée par SimbiotX permet aussi d’extrapoler les expériences toxicologiques in vitro sur l’humain. Un sujet sur lequel l’équipe est en étroite collaboration avec le département de toxicologie du IfADo Leibniz Institute (Allemagne). Prenons par exemple un cas de surdosage en paracétamol. Celui-ci entraîne la mort des hépatocytes entourant la veine centrale de chaque lobule du foie, puis leur rapide régénération. En simulant numériquement chaque cellule hépatique individuelle, l’équipe crée un jumeau virtuel de portion de foie permettant de déterminer si et dans quelles conditions les mécanismes hypothétiques expliquent les données d'observation (par exemple la dose-dépendance de la zone affectée).
Si l’hypothèse émise ne colle pas à l’observation clinique, les modèles peuvent tester des mécanismes alternatifs et aider à la conception des expériences à mener sur l’animal pour obtenir confirmation des hypothèses. « Une fois qu'un modèle a été correctement paramétré et validé par des données, il peut être utilisé pour simuler l'influence de différentes perturbations, comme des manipulations moléculaires, ou le blocage de l'expression de certains gènes dont les effets sur l’organe et la fonction modélisés sont connus » détaille Dirk Drasdo. En aidant l’expérimentateur à déterminer quelles expériences ont le plus d’influence sur ce qu’il peut mesurer, ces modèles participent donc à la réduction du nombre d’expériences à faire, et notamment d’expérimentations animales.
SimbiotIx, lauréat des Trophées de l'Innovation et de la Transformation Numérique 2023 – © Solutions numériques
Amener l’innovation au cœur du bloc opératoire
En réponse directe aux questions cliniques, Irène Vignon-Clementel développe des outils numériques pour essayer d’appréhender les risques chirurgicaux, au départ pour les opérations des maladies congénitales du cœur. Dans ce cadre, elle a notamment collaboré avec l’Hôpital pédiatrique de Stanford (États-Unis), et l’Hôpital Necker-Enfants malades.
Depuis plusieurs années, elle partage l’intérêt de Dirk Drasdo pour le foie, et ses chirurgies (résection, transplantation…), avec l’objectif commun de générer un modèle numérique de l’organe qui recouvre de nombreux niveaux d’organisation, de la cellule individuelle à l’organe fonctionnel, avec son architecture en lobules et sa circulation sanguine. « S’il existe depuis peu des modèles anatomiques et des algorithmes multiparamétriques d’aide à la décision, ceux-ci sont peu précis pour anticiper les suites opératoires, entre autres parce qu’ils ne prennent pas en compte la dynamique de la circulation sanguine du patient » explique la chercheuse.
Au sein de SimbiotX, et en collaboration avec des cliniciens, elle cherche à mettre au point de tels modèles, dits "hémodynamiques" pour prédire la réaction d’un foie particulier à une ablation partielle, en fonction de la re-répartition du débit et de la pression sanguine. C’est notamment l’enjeu de son partenariat avec l’équipe d’Eric Vibert, professeur de chirurgie à l’Université Paris-Saclay au sein du Centre-hépatobiliaire de l’hôpital APHP Paul Brousse.
« En utilisant la puissance des mathématiques pour analyser le réel sans le simplifier, cette collaboration a permis d’améliorer notre compréhension de l’hémodynamique. Au bloc opératoire, cela se traduit par une meilleure anticipation des conséquences de nos actes chirurgicaux, et une meilleure sélection des malades opérables », précise le clinicien.
Vers une chirurgie personnalisée
Pour l’instant, ces modèles sont utilisés de façon rétrospective, pour comprendre a posteriori les changements de flux sanguins provoqués par les opérations. Mais la chercheuse espère que « d’ici cinq à dix ans, ils soient suffisamment prédictifs et validés pour être utilisés par des cliniciens experts pour planifier leurs opérations ». Elle a d’ailleurs reçu fin 2019 une bourse ERC pour son projet MoDeLLiver de modèle hémodynamique pour la planification des interventions chirurgicales des poumons et du foie.
En mettant à profit la puissance de la modélisation mathématique, SIMBIOTX permet donc d’identifier les mécanismes qui régissent le fonctionnement du corps humain, depuis son échelle cellulaire jusqu’aux organes entiers, et au système sanguin qui les irrigue. Les domaines d’application s’étendent également vers la biotechnologie, la création de prothèses… L'un des principaux points forts de ces modèles est qu'ils permettent d'étudier l'interaction complexe de la biomécanique des tissus et des cellules, de la biochimie, ainsi que des flux à plusieurs échelles. « Le prix à payer est qu'ils nécessitent la manipulation d'un code complexe. Mais si nous avions plus de forces vives, nous pourrions faire encore plus et plus vite, car nous recevons de très nombreuses sollicitations de cliniciens », glisse Irène Vignon-Clementel. Avis aux financeurs…
En savoir plus sur les recherches de l'équipe SimbiotX
- Optimizing cancer drug therapies, Inria, 08/02/2021.
- Irene Vignon-Clementel & Stéphane Cotin - Le numérique, appui au contrôle de risque en chirurgie, Fondation Inria, 04/01/2021.
- MOX Colloquium : Irene Vignon-Clementel, « Patient-specific hemodynamics simulations for interventional planning of congenital and acquired cardiac diseases », Laboratorio MOX, 21/01/2021.
- Jumeaux numériques en santé, mirage ou réalité ?, Institut Mines-Télécom, 28/01/2019.